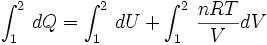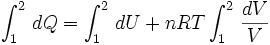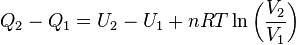Expansión
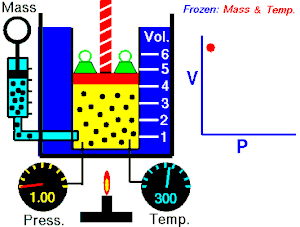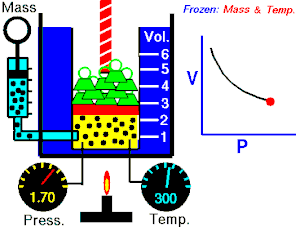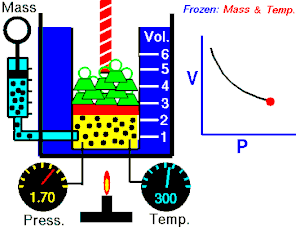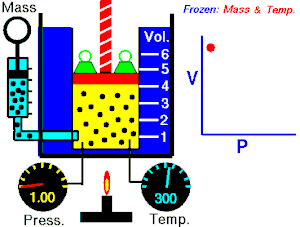
Se denomina proceso isotérmico o proceso isotermo al cambio reversible en un sistema termodinámico, siendo dicho cambio a temperatura constante en todo el sistema. La compresión o expansión de un gas ideal puede llevarse a cabo colocando el gas en contacto térmico con otro sistema de capacidad calorífica muy grande y a la misma temperatura que el gas. este otro sistema se conoce como foco calórico. De esta manera, el calor se transfiere muy lentamente, permitiendo que el gas se expanda realizando trabajo. Como la energía interna de un gas ideal sólo depende de la temperatura y ésta permanece constante en la expansión isoterma, el calor tomado del foco es igual al trabajo realizado por el gas: Q = W.
Una curva isoterma es una línea que sobre un diagrama representa los valores sucesivos de las diversas variables de un sistema en un proceso isotermo. Las isotermas de un gas ideal en un diagrama P-V, llamado diagrama de Clapeyron, son hipérbolas equiláteras, cuya ecuación es P•V = constante.
Una expansión isotérmica es un proceso en el cual un gas se expande (o contrae), manteniendo la temperatura constante durante dicho proceso, es decir que T1 = T2 para los estados inicial (1) y final (2) del proceso isotérmico. Aplicando el primer principio de la termodinámica se obtiene:
Entonces integrando la expresión anterior, tomando como estado inicial el estado 1 y estado final el estado 2, se obtiene:
 ..........(1)
..........(1)
Por la definición de trabajo dada en mecánica se tiene que:
Pero la fuerza  se puede expresar en función de la presión que se ejerce el gas, y el desplazamiento
se puede expresar en función de la presión que se ejerce el gas, y el desplazamiento 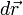 se puede escribir como dx, entonces:
se puede escribir como dx, entonces:
 se puede expresar en función de la presión que se ejerce el gas, y el desplazamiento
se puede expresar en función de la presión que se ejerce el gas, y el desplazamiento 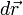 se puede escribir como dx, entonces:
se puede escribir como dx, entonces:
Pero Adx equivale a dV, el aumento en el volumen del gas durante esta pequeña expansión, entonces el trabajo efectuado por el gas sobre los alrededores como resultado de la expansión es:
 ..........(2)
..........(2)
Ahora reemplazando (1) en (2) se puede integrar:
 ..........(3)
..........(3)
Pero para integrar la tercera integral, es necesario conocer la forma de variación de la presión P con el volumen, durante el proceso tratado.
En el caso de tratar con gases ideales, se tendría la relación:
 ..........(4)
..........(4)
Por lo tanto reemplazando (4) en (3) se tiene que:
Como los valores n y R son constantes para cada gas ideal, y en este caso la temperatura también es constante, éstas pueden salir fuera de la integral obteniéndose:
Ahora integrando:
![[Q]_1^2 = [U]_1^2 + nRT[\ln V]_1^2](https://upload.wikimedia.org/math/9/b/b/9bb7def5b45c1c793290a37d2aafc98d.png)
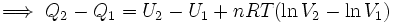
 ..........(5)
..........(5)
Pero se sabe que la energía interna depende sólo de la temperatura (Ver: La energía interna como función de la temperatura), y como en este proceso ésta se mantiene constante, no hay cambio en la energía interna del gas, por lo que la expresión (5) se reduce a:
Por lo tanto, en una expansión isotérmica de un gas perfecto, el calor de entrada es igual al trabajo efectuado por el gas.
Forma
En los gases, las fuerzas que mantienen unidas las partículas son muy pequeñas. En un gas el número de partículas por unidad de volumen es también muy pequeño.
Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que los contiene. Esto explica las propiedades de expansibilidad y compresibilidad que presentan los gases: sus partículas se mueven libremente, de modo que ocupan todo el espacio disponible. La compresibilidad tiene un límite, si se reduce mucho el volumen en que se encuentra confinado un gas éste pasará a estado líquido.
Volumen
El volumen es el espacio que ocupa un sistema. Recuerda que los gases ocupan todo el volumen disponible del recipiente en el que se encuentran. Decir que el volumen de un recipiente que contiene un gas ha cambiado es equivalente a decir que ha cambiado el volumen del gas.
En el laboratorio se utilizan frecuentemente jeringuillas como recipientes de volumen variable cuando se quiere experimentar con gases.
Compresibilidad
La compresibilidad es una propiedad de la materia a la cual se debe que todos los cuerpos disminuyan de volumen al someterlos a una presión o compresión determinada manteniendo constantes otros parámetros.
En general para un sistema estable, la compresibilidad es un número positivo, lo que significa que cuando se aumenta la presión sobre el sistema, este disminuye su volumen. El caso contrario se puede observar en sistemas inestables por ejemplo en un sistema químico cuando la presión inicia una explosión. Los sólidos a nivel molecular son muy difíciles de comprimir, ya que las moléculas que tienen los sólidos están muy pegadas y existe poco espacio libre entre ellas como para acercarlas sin que aparezcan fuerzas de repulsión fuertes. Esta situación contrasta con la de los gases los cuales tienen sus moléculas muy separadas y que en general son altamente compresibles bajo condiciones de presión y temperatura normales. Los líquidos bajo condiciones de temperatura y presión normales son también bastante difíciles de comprimir aunque presenta una pequeña compresibilidad mayor que la de los sólidos.
En termodinámica se define la compresibilidad de un sistema termodinámico como el cambio relativo de volumen frente a una variación de la presión. En principio la magnitud de la compresibilidad depende de las condiciones bajo las cuales se lleva a cabo la compresión o descompresión del sistema, por lo que a menos que se especifique el modo en que se lleva a cabo esa operación la compresibilidad de un valor u otro según las cantidades de calor intercambiadas con el exterior. Debido a esa dependencia de la compresibilidad de las condiciones se distingue entre la compresibilidad isoterma y la compresibilidad adiabática.
Es una medida de la compresibilidad de un cuerpo o sistema termodinámico cuando se somete a un proceso termodinámico de transformación cuasiestática de presión mientras su temperatura se mantiene constante y uniforme, viene dada por:
En un proceso de variación de presión a temperatura constante, el cuerpo habrá intercambiado una cierta cantidad de calor con el exterior por lo que su energía total, que puede obtenerse como suma del trabajo realizado sobre el cuerpo y del calor intercambiado por el mismo no permanecerá constante.En un proceso adiabático de variación de presión, el cuerpo experimentará algún cambio de temperatura. Todos los fluidos son compresibles, incluyendo los líquidos. Cuando estos cambios de volumen son demasiado grandes se opta por considerar el flujo como compresible (que muestran una variación significativa de la densidad como resultado de fluir), esto sucede cuando la velocidad del flujo es cercano a la velocidad del sonido. Estos cambios suelen suceder principalmente en los gases ya que para alcanzar estas velocidades de flujo en líquidos, se precisa de presiones del orden de 1000 atmósferas, en cambio un gas sólo precisa una relación de presiones de 2:1 para alcanzar velocidades sónicas. La compresibilidad de un flujo es básicamente una medida en el cambio de la densidad. Los gases son en general muy compresibles, en cambio, la mayoría de los líquidos tienen una compresibilidad muy baja. Por ejemplo, una presión de 500 kPa provoca un cambio de densidad en el agua de solamente 0,024% (a temperatura ambiente). En cambio, esta misma presión aplicada al aire provoca un cambio de densidad de 250%. Por esto normalmente al estudio de los flujos compresibles se le conoce como dinámica de gases, siendo esta una nueva rama de la mecánica de fluidos, la cual describe estos flujos.
En un flujo usualmente hay cambios en la presión, asociados con cambios en la velocidad. En general, estos cambios de presión inducirán a cambios de densidad, los cuales influyen en el flujo, si estos cambios son importantes los cambios de temperatura presentados son apreciables. Aunque los cambios de densidad en un flujo pueden ser muy importantes hay una gran cantidad de situaciones de importancia práctica en los que estos cambios son despreciables.
El flujo de un fluido compresible se rige por la primera ley de la termodinámica en los balances de energía y con la segunda ley de la termodinámica, que relaciona la transferencia de calor y la irreversibilidad con la entropía. El flujo es afectado por efectos cinéticos y dinámicos, descritos por las leyes de Newton, en un marco de referencia inercial –aquel donde las leyes de Newton son aplicables-. Además, el flujo cumple con los requerimientos de conservación de masa. Es sabido que muchas propiedades, tales como la velocidad del fluido en un tubo, no son uniformes a lo largo de la corriente.
Presión
En el marco de la teoría cinética, la presión de un gas es explicada como el resultado macroscópico de las fuerzas implicadas por las colisiones de las moléculas del gas con las paredes del contenedor. La presión puede definirse por lo tanto haciendo referencia a las propiedades microscópicas del gas.
En efecto, para un gas ideal con N moléculas, cada una de masa m y moviéndose con una velocidad aleatoria promediovrms contenido en un volumen cúbico V, las partículas del gas impactan con las paredes del recipiente de una manera que puede calcularse de manera estadística intercambiando momento lineal con las paredes en cada choque y efectuando unafuerza neta por unidad de área, que es la presión ejercida por el gas sobre la superficie sólida.
La presión puede calcularse como:
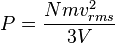 (gas ideal)
(gas ideal)Este resultado es interesante y significativo no solo por ofrecer una forma de calcular la presión de un gas sino porque relaciona una variable macroscópica observable, la presión, con la energía cinética promedio por molécula, 1/2 mvrms², que es una magnitud microscópica no observable directamente. Nótese que el producto de la presión por el volumen del recipiente es dos tercios de la energía cinética total de las moléculas de gas contenidas.
Densidad
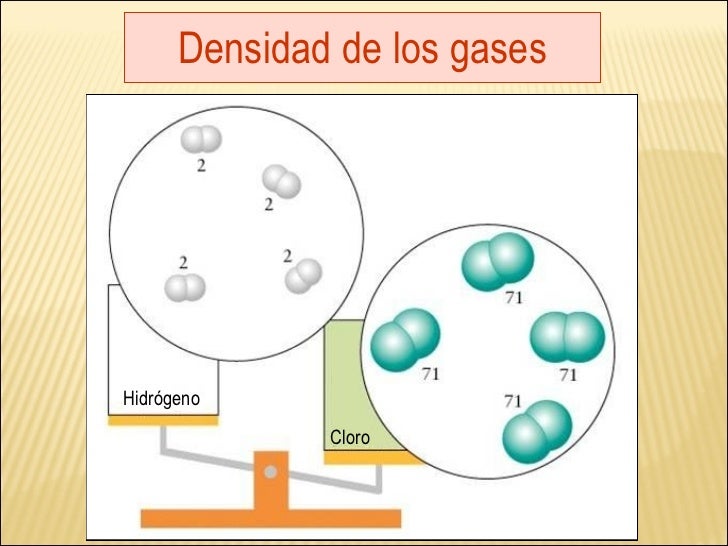
Densidad: Masa por unidad de volumen de un material. El término es aplicable a mezclas y sustancias puras y a la materia en el estado solidó, líquido y gaseoso. Las unidades comunes de la densidad relativa (gravedad específica) para los gases puede ser aire a la temperatura y presión estándar.
Ahora que ya sabes que es la densidad, en general vamos hablar sobre lo que significa densidad de un gas ya que es la parte importante de nuestra practica.
Densidad de un gas:En un determinado volumen las moléculas de gas ocupan cierto espacio por lo tanto se distribuirán de manera que encontremos menor cantidad en el mismo volumen anterior. Podemos medir la cantidad de materia, ese número de moléculas, mediante una magnitud denominada masa. La cantidad de moléculas, la masa, no varía al aumentar o disminuir (como en este caso) el volumen, lo que cambia es la relación masa - volumen. Esa relación se denomina densidad (d). La densidad es inversamente proporcional al volumen (al aumentar al doble el volumen, manteniendo constante la masa, la densidad disminuye a la mitad) pero directamente proporcional a la masa (si aumentamos al doble la masa, en un mismo volumen, aumenta al doble la densidad).
La materia se puede presentar en sus tres estados (solidó, liquido y gaseoso) en esta ultima se encuentra las sustancias que común mente denominamos gases lo que denominamos gases. Entonces vamos a relación esto con las siguientes leyes.
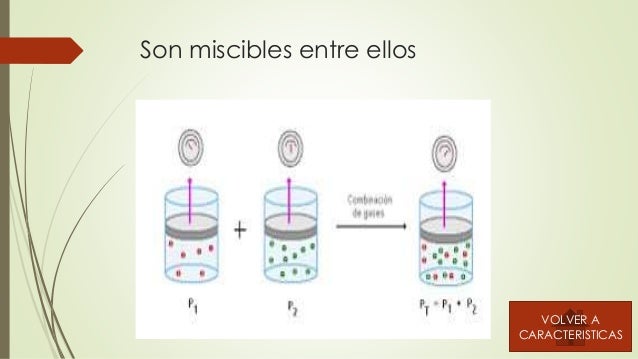
Miscibilidad
Miscibilidad es un término usado en química que se refiere a la propiedad de algunos líquidos para mezclarse en cualquier proporción, formando una disolución. En principio, el término es también aplicado a otras fases (sólidos, gases), pero se emplea más a menudo para referirse a la solubilidad de un líquido en otro. El agua y el etanol (alcohol etílico), por ejemplo, son miscibles en cualquier proporción.
Por el contrario, se dice que las sustancias son inmiscibles si en alguna proporción no son capaces de formar una fase homogénea. Por ejemplo, el éter etílico es en cierta medida soluble en agua, pero a estos dos solventes no se les considera miscibles dado que no son solubles en todas las proporciones.
En los compuestos orgánicos, el porcentaje del peso de la cadena de hidrocarburos con frecuencia determina la miscibilidad del compuesto con agua. Por ejemplo, entre los alcoholes, el etanol tiene dos átomos de carbono y es miscible con agua, mientras que el 1-octanol (C8 H18 O) no lo es. Este es también el caso de los lípidos; las largas cadenas que caracterizan a los lípidos son la causa de que estos casi siempre sean inmiscibles con agua. Algo similar ocurre con otros grupos funcionales. El ácido acético es miscible con agua, y en la situación contraria se encuentra el ácido valérico (C4 H9 CO2 H). Los aldehídos simples y las cetonas tienden a ser miscibles con agua, ya que un puente de hidrógeno se puede formar entre el átomo de hidrógeno de una molécula de agua y el par de electrones del átomo de oxígeno carbonilo.
La miscibilidad es parcialmente una función de la entropía, y por lo tanto se observa más comúnmente en los estados de la materia que poseen más entropía. Los gases se mezclan con bastante facilidad, pero los sólidos raramente son miscibles. Dos excepciones notables a esta regla son las soluciones sólidas de cobre con níquel (el cuproníquel resultante es usado para la fabricación de monedas y tuberías) , y las de silicio con germanio usadas en electrónica. Las sustancias con entropía configuracional extremadamente baja, los polímeros especialmente, tienen poca probabilidad de ser miscibles entre sí incluso en el estado líquido. Dos sustancias son miscibles si la mezcla tiene como resultado una menor energía libre que cada uno de los componentes por separado.
La miscibilidad es parcialmente una función de la entropía, y por lo tanto se observa más comúnmente en los estados de la materia que poseen más entropía. Los gases se mezclan con bastante facilidad, pero los sólidos raramente son miscibles. Dos excepciones notables a esta regla son las soluciones sólidas de cobre con níquel (el cuproníquel resultante es usado para la fabricación de monedas y tuberías) , y las de silicio con germanio usadas en electrónica. Las sustancias con entropía configuracional extremadamente baja, los polímeros especialmente, tienen poca probabilidad de ser miscibles entre sí incluso en el estado líquido. Dos sustancias son miscibles si la mezcla tiene como resultado una menor energía libre que cada uno de los componentes por separado.